
当研究室に関する記事やインタビュー、研究のプレスリリースを以下にまとめました。
■2021年
宇都宮大学ホームページに掲載された蚕糸学会賞受賞の記事
「農学部の岩永将司准教授が令和3年度日本蚕糸学会賞を受賞しました」

農学部生物資源科学科の岩永将司准教授が令和3年度日本蚕糸学会賞を受賞しました。受賞対象研究は「昆虫由来培養細胞に潜在感染する Bombyx mori latent virusに関する研究」です。岩永准教授は「昆虫ウイルスと宿主の相互作用の解明」を研究テーマとしており、今回の受賞は「培養細胞に潜在感染しているウイルスの解析という基礎的な側面と、産業利用されている培養細胞に混入している潜在感染ウイルスの安全性評価や不活化法という応用的な側面」が評価されました。
「Bombyx mori latent virusは、宿主細胞に潜在感染し、宿主を致死させることなく、ただひたすらに増殖し続ける持続感染型のウイルスです。このウイルスの研究をここ10年ほど研究室の学生さんたちと続けてきたことが評価されたことは大変うれしいことです。」と受賞の喜びを語りました。
昆虫培養細胞は組換えタンパク質発現系などで医薬品の製造にも利用されています。そのため、培養細胞の中に潜在感染しているウイルスは大きな脅威にもなり得ます。一方で、潜在感染は宿主の生体防御機構をかいくぐって成立させているものであり、非常に興味深いウイルスと宿主の相関が存在します。岩永准教授らは、Bombyx mori latent virusの安全性の評価や不活化法を開発しただけでなく、本ウイルスに対する宿主側の生体防御機構がsiRNAによるサイレンシングだけでなくpiRNAによるサイレンシングを受けていること、そして共感染している他のウイルスとも相互作用して別種のウイルス封入体に相乗りすることを明らかにしました。「これからも、学生さんと楽しく研究していきたいと考えています」と話しています。
■2019年
宇都宮大学ホームページに掲載された研究に関するプレスリリース

発表者
津久井 啓多†(宇都宮大学大学院農学研究科 生物生産科学専攻 修士課程2年;当時)
八木沢 千尋†(宇都宮大学農学部生物資源科学科4年;当時)
藤本 正太†(東京農工大学大学院連合農学研究科 生物生産科学専攻 博士課程3年)
小川 茂恵(宇都宮大学農学部生物資源科学科4年;当時)
國生 龍平(東京大学大学院農学生命科学研究科研究員;当時)
野澤 瑞佳(大日本蚕糸会蚕業技術研究所 主任研究員)
川崎 秀樹(宇都宮大学農学部生物資源科学科 名誉教授)
勝間 進(東京大学大学院農学生命科学研究科 生産・環境生物学専攻 准教授)
岩永 将司*(宇都宮大学農学部生物資源科学科 准教授)(†筆頭著者、*責任著者)
概要
宇都宮大学農学部の岩永将司准教授らのグループは、カイコ培養細胞へ持続感染しているBombyx mori latent virus(BmLV)が、別種であるバキュロウイルス(カイコ核多角体病ウイルス)の形成するウイルス封入体に感染性を維持したまま取り込まれることを見出しました。これは、BmLVがバキュロウイルスの封入体に“相乗り”していることを示しており、ウイルス同士が相互作用する新たな形として興味深いものです。この発見を足がかりにして、今後、BmLVのライフサイクルの解明や、他のウイルスにおける“相乗り”現象の発見が期待されます。
発表内容
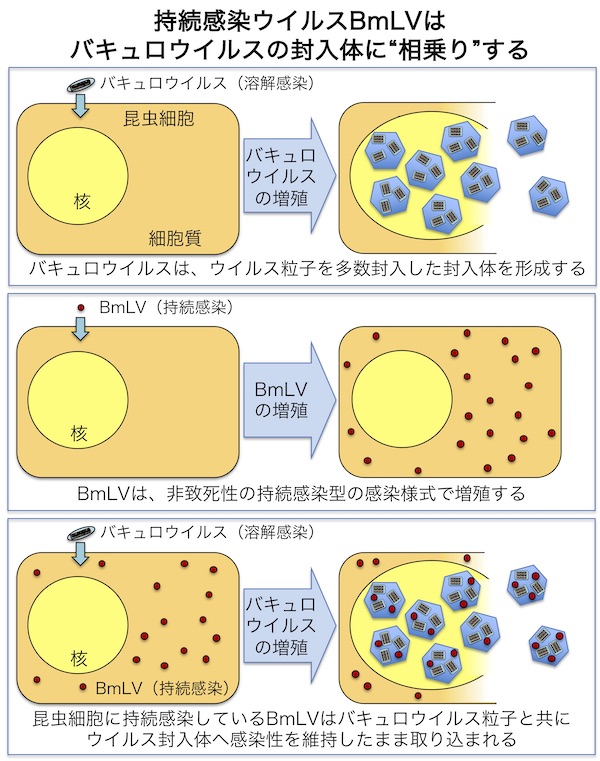
ウイルスの感染には、ウイルスの放出後に宿主細胞が致死に至る溶解感染だけでなく、ウイルスの放出を伴わずに宿主が生存する潜伏感染、そしてウイルスが放出されつつも宿主が生存する持続感染があります。チョウ目昆虫のカイコに感染するカイコバキュロウイルスは、代表的な溶解感染型の昆虫ウイルスであり、感染後、4-5日で宿主の核内に多数の結晶体を形成します。これはウイルス封入体と呼ばれ、この封入体の中には多数の小さなウイルス粒子が埋め込まれ、紫外線を始めとする厳しい野外環境からウイルス粒子を保護する働きがあります(図上段)。一方で、Bombyx mori latent virus(BmLV)は代表的な持続感染型の昆虫ウイルスであり、カイコ由来の培養細胞で宿主に病徴を呈さずに増殖しています(図中段)。興味深いことに、BmLVは既に樹立されたほとんど全てのカイコ由来培養細胞に混入しているにも関わらず、その遺伝子配列は植物ウイルスであるチモウイルス科マキュラウイルス属のグループに最も近縁です。このことから、BmLVは見た目が植物ウイルスであるにも関わらず、何らかのメカニズムによって昆虫の培養細胞で増殖するようになった“植物ウイルス様昆虫ウイルス”であると考えられています。近年、BmLVの持続感染メカニズムに関して解明が進み、BmLVの持続感染が2種類の小分子RNAによって制御されていることが明らかになりました(2018年1月19日;宇都宮大学プレスリリース「見た目は植物ウイルス、でも昆虫細胞に持続感染しているウイルスの謎を解明」)。しかしながら、BmLVのライフサイクルについては明らかになっていませんでした。
今回、宇都宮大学農学部生物資源科学科の岩永将司准教授らのグループは、東京大学大学院農学生命科学研究科、大日本蚕糸会蚕業技術研究所との共同研究によって、持続感染型のBmLVと溶解感染型のバキュロウイルスの共感染実験を行いました。その結果、培養細胞におけるBmLVの持続感染がバキュロウイルスの増殖に影響を及ぼすこと、また、培養細胞でのみ増殖しカイコ幼虫では増殖しなかったBmLVが、バキュロウイルスとの共感染によってカイコ幼虫においても増殖しうることを見出しました。更に解析を進めたところ、BmLVとの共感染細胞で産生されたバキュロウイルスの封入体の中に、BmLVの粒子がバキュロウイルス粒子と共に封入されていることも明らかとなりました(図下段)。驚くべきことに、封入体に埋め込まれていたBmLVは感染性を保持したままであり、培養細胞への接種試験によって再び増殖することも明らかとなりました。これは、BmLVがバキュロウイルスの構築する封入体に“相乗り”していたことを示します。一方で、このような“相乗り”は培養細胞でのみ観察され、カイコ幼虫では認められませんでした。これは、BmLVが培養細胞で豊富に増殖しているのに対して、カイコ幼虫では効率的に増殖できないためであると考えられました。そのため、BmLVとバキュロウイルスの相関は培養細胞でのみ生じている現象であると考えられます。
本研究成果により、封入体への“相乗り”という、BmLVとバキュロウイルスの新たな相関の形が明らかとなりました。近年、BmLVに類縁性を有する様々な持続感染型ウイルスがカイコ培養細胞だけでなく、ハチ、ダニ、蚊などから単離されています。今後、これらの“植物ウイルス様昆虫ウイルス”と同一個体に感染する溶解感染型ウイルスとの間に、どのような相関の形があるのか興味が持たれます。本研究は、文部科学省科学研究費補助金(16K08095、25450482、16H05051)による支援を受けて行われました。
発表雑誌名 Viruses
論文タイトル Infectious virions of Bombyx mori latent virus are incorporated into Bombyx mori nucleopolyhedrovirus occlusion bodies
著者 Tsukui K.†, Yagisawa C.†, Fujimoto S.†, Ogawa M., Kokusho R., Nozawa M., Kawasaki H., Katsuma S., Iwanaga M.* (†筆頭著者、*責任著者)
■2018年
宇都宮大学ホームページに掲載された研究に関するプレスリリース

概要
宇都宮大学農学部の岩永将司准教授らのグループは、カイコマキュラウイルス(Bombyx mori macula-like virus)に感染したカイコ培養細胞におけるトランスクリプトーム解析によって、マキュラウイルスの持続感染が、宿主のsmall interfering RNA (siRNA)、およびPIWI-interacting RNA (piRNA)という2 種類の小分子RNAによって制御されていることを発見しました。すなわち、これら2つの経路による制御が持続感染成立のコアメカニズムの一端を担っていることを明らかにしました。この発見を足がかりにして、今後、マキュラウイルスの増殖メカニズムの解明や新たな遺伝子発現ベクターの開発が期待されます。
本研究成果は2018(平成30年)1月17日、科学雑誌「DNA Research」オンライン版に掲載されました。
発表内容
ウイルスの感染には、ウイルスの放出後に宿主細胞が致死に至る溶解感染だけでなく、ウイルスの放出を伴わずに宿主が生存する潜伏感染、そしてウイルスが放出されつつも宿主が生存する持続感染があります。カイコマキュラウイルスは、2005年に本グループがカイコ卵巣由来培養細胞から発見したプラス鎖RNAをゲノムとして有する持続感染型のウイルスです。興味深いことに、本ウイルスは既に樹立されたほとんど全てのカイコ由来培養細胞に混入しているにも関わらず、その遺伝子配列は植物ウイルスであるチモウイルス科マキュラウイルス属のグループに最も近縁です。このことから、本ウイルスは見た目が植物ウイルスであるにも関わらず、何らかのメカニズムによって昆虫の培養細胞で増殖するようになったと考えられます。しかし、本ウイルスはカイコ個体からは検出されておらず、本ウイルスの混入源や生活環、そして持続感染成立に関するメカニズムについては未解明のままでした。
今回、宇都宮大学農学部生物資源科学科の岩永将司准教授らのグループは、東京大学大学院農学生命科学研究科、同新領域創成科学研究科、同分子細胞生物学研究所のグループとの共同研究によって、マキュラウイルスに感染したカイコ培養細胞のRNAシークエンス解析を行いました。その結果、ウイルスの増殖に伴って転写量が増減する150の宿主由来の転写物を同定しました。増加する転写物の中には細胞接着因子も含まれていましたが、これはマキュラウイルスの増殖に伴って観察される宿主細胞集塊の形成に関与するものと考えられました。また、マキュラウイルスに由来する転写物は全転写物の15%以上を占めており、本ウイルスが持続感染にも関わらず非常に高いレベルで増殖していることが示されました。特に、サブゲノミックRNAと呼ばれる領域の転写量が多く、この領域にコードされるp15遺伝子がウイルスの増殖に必須であることも明らかとなりました。
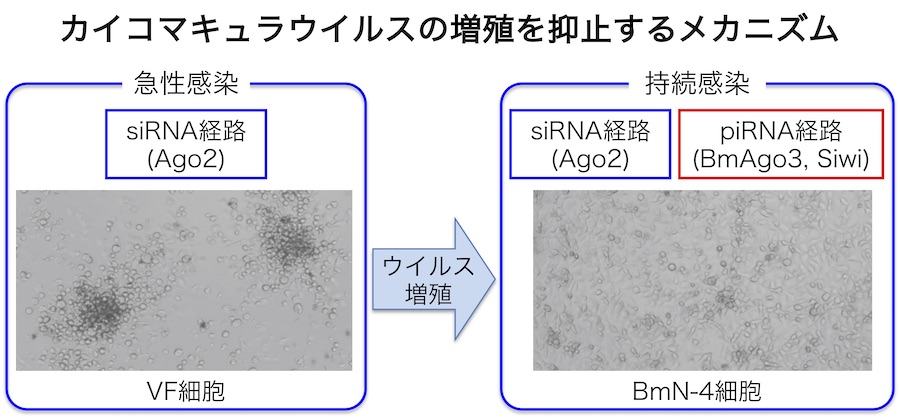
一般にウイルスに感染した宿主細胞では、ウイルスRNAを元にsmall interfering RNA (siRNA)と呼ばれるウイルス由来の小分子RNAが生成され、siRNAと相補的な配列を有するウイルスの増殖を抑えることが知られています。この現象はRNAサイレンシングと呼ばれています。マキュラウイルスが持続感染している培養細胞を用いて小分子RNAを解析したところ、ウイルスが持続感染している細胞では、ウイルス由来の小分子RNAが存在することが明らかとなりました。詳細な解析を行ったところ、ウイルスゲノム全体からsiRNAが作られていただけではなく、近年、トランスポゾンの制御や性決定で着目されているPIWI-interacting RNA (piRNA)と呼ばれる新しいクラスの小分子RNAが主にサブゲノムRNA領域から作られていることが明らかとなりました。そこで、siRNA経路に関与するAgo2と、piRNA経路に関与するSiwi、BmAgo3を、ウイルスが既に持続感染している細胞(持続感染細胞)と、新たにウイルスを接種した細胞(急性感染細胞)のそれぞれでRNA干渉によってノックダウンしました。その結果、持続感染細胞ではAgo2、Siwi、Ago3ノックダウンの全てでウイルスRNAの増加が見られたのに対し、急性感染細胞ではAgo2ノックダウンのみでウイルスRNAが増加しました。以上の結果から、マキュラウイルスの感染においては、まずsiRNA経路によってウイルスが抑制され、それでもウイルスの増殖が抑制できなかった場合にはpiRNA経路も利用して抑制すること、このようにしてウイルスの増殖と抑止が拮抗した状態がマキュラウイルスの持続感染につながることが示唆されました。
本研究成果により、マキュラウイルスの増殖に伴って転写量が変動する多数の遺伝子が同定され、また、異なる2つの小分子RNA経路がウイルス増殖の抑止に関与していることが明らかとなりました。これは、マキュラウイルスの持続感染成立に関するコアメカニズムの一端を解明しただけでなく、近年注目を集めているpiRNAの新たな機能の解明という点で重要です。本研究は、文部科学省科学研究費補助金(基盤研究A、基盤研究B、基盤研究C、及び新学術領域研究)による支援を受けて行われました。
発表雑誌名 DNA Research
論文タイトル Transcriptome profiling reveals infection strategy of an insect maculavirus
著者 Katsuma S.†*, Kawamoto M.†, Shoji K.†, Aizawa T.†, Kiuchi T., Izumi N., Ogawa M., Mashiko T., Kawasaki H., Sugano S., Tomari Y., Suzuki Y., and Iwanaga M.* (†These authors contributed equally to this work, *co-corresponding authors)
■2017年
UUnow(宇都宮大学広報誌)第44号に掲載されたインタビュー


■2017年
峰が丘同窓会会報第155号に掲載された研究紹介

